DISPOSITIVOS MÉDICOS
CONTROL DE FUGAS
En la industria médica, el control de fugas es un proceso crítico de control de calidad para garantizar
el funcionamiento de los dispositivos, la seguridad del paciente y el cumplimiento normativo.
POR QUÉ EL CONTROL DE FUGAS ES ESENCIAL PARA LOS DISPOSITIVOS MÉDICOS
Los dispositivos médicos suelen contener fluidos, gases o volúmenes sellados y pueden suministrarse en envases estériles. Cualquier pérdida de integridad puede provocar:
- compromiso del rendimiento del dispositivo
- pérdida de esterilidad
- incumplimiento normativo
- mayor riesgo para la seguridad del paciente
El control de fugas verifica que cada dispositivo cumpla sus requisitos funcionales, de seguridad y normativos antes de su comercialización.
Los métodos no destructivos permiten a los fabricantes probar los productos sin dañarlos, facilitando una inspección al 100 %, trazabilidad completa y reducción de desechos.
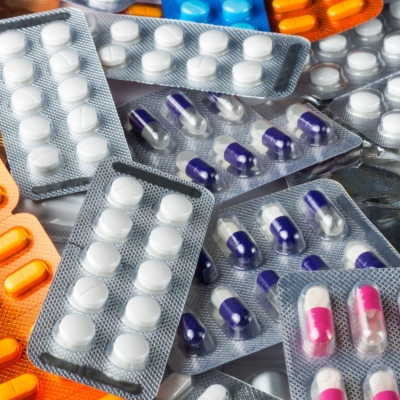
¿QUÉ PRODUCTOS MÉDICOS PUEDEN SOMETERSE A CONTROL DE FUGAS?
Tanto la integridad del dispositivo como la integridad de la barrera estéril pueden verificarse mediante tecnologías no destructivas.
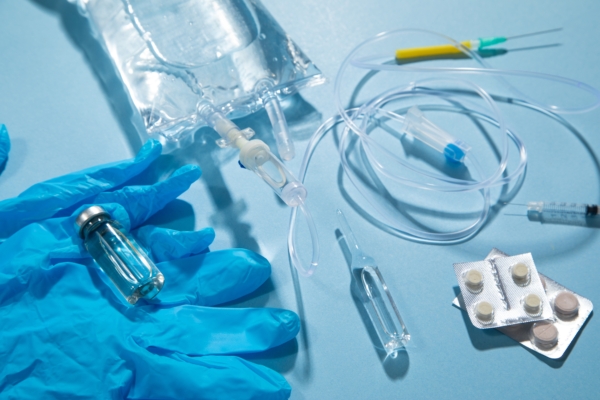
SEGURIDAD MÉDICA Y FARMACÉUTICA
Las operaciones de control de fugas se realizan en entornos controlados donde la seguridad del operador y el control de la contaminación son esenciales.
En la fabricación médica y farmacéutica, los operadores pueden estar expuestos a:
- agentes químicos de limpieza y desinfección
- principios activos farmacéuticos (API)
- partículas, vapores o aerosoles
El uso de equipos de protección individual (EPI) adecuados ayuda a proteger a los trabajadores, manteniendo al mismo tiempo la calidad del producto y el control del proceso.
Un programa estructurado de EPI incluye:
- protección respiratoria con pruebas de ajuste adecuadas
- protección ocular y facial
- ropa y guantes de protección
- formación sobre el uso y mantenimiento correctos
Las prácticas de trabajo seguras contribuyen directamente a un control de fugas fiable y a una calidad de producción constante.
TECNOLOGÍAS NO DESTRUCTIVAS DE CONTROL DE FUGAS
ATEQ ofrece varias tecnologías complementarias, seleccionadas según el diseño del dispositivo, los materiales, el volumen interno, la tasa de fuga objetivo y las limitaciones de producción.
CUMPLIMIENTO DE NORMAS Y REGULACIONES MÉDICAS
ISO13485 exige a los fabricantes de dispositivos médicos implementar procesos de inspección controlados y validados.
Los sistemas de control de fugas de ATEQ respaldan:
- Calificación de instalación (IQ)
- Calificación operacional (OQ)
- Calificación de desempeño (PQ)
- Trazabilidad completa de los resultados de ensayo
ISO 11607 define los requisitos para los materiales, sistemas y procesos de envasado estéril.
El control de fugas desempeña un papel clave para demostrar que la barrera estéril mantiene su integridad hasta el momento de uso.
Las pruebas por caída de vacío se utilizan comúnmente como parte de las estrategias de cumplimiento de ISO 11607.
Los límites de fuga aceptables se definen mediante un enfoque basado en el riesgo de acuerdo con ISO 14971.
Los umbrales de fuga se correlacionan con modos de fallo críticos y condiciones reales de uso para garantizar la seguridad del paciente.
Las soluciones de control de fugas de ATEQ respaldan el cumplimiento de las expectativas de la FDA y los requisitos del MDR de la UE, facilitando el acceso al mercado mundial para los fabricantes de dispositivos médicos.
¿POR QUÉ ELEGIR ATEQ?
ATEQ apoya a los fabricantes de dispositivos médicos en cada etapa del ciclo de vida del producto, ayudando a garantizar la seguridad, el cumplimiento normativo y el rendimiento.
NUESTROS PRODUCTOS
NUESTROS FOLLETOS
Preguntas frecuentes
El control de fugas no destructivo es un método de control de calidad utilizado para detectar fugas sin dañar el dispositivo médico ni su envase.
Garantiza la integridad funcional del dispositivo y, cuando corresponde, la integridad del sistema de barrera estéril, permitiendo que el producto probado siga siendo utilizable.
Este enfoque es esencial en la fabricación médica, donde la seguridad, la trazabilidad y el cumplimiento normativo son críticos.
El control de fugas se aplica comúnmente a:
- catéteres, tubos y equipos de transferencia de fluidos
- balones, reservorios y dispositivos flexibles
- válvulas, conectores y conjuntos sellados
- dispositivos médicos implantables o de un solo uso
- envases estériles como blísteres, bolsas y bandejas
Debe probarse cualquier dispositivo en el que una fuga pueda afectar a la seguridad del paciente, el rendimiento o la esterilidad.
Los ensayos no destructivos permiten a los fabricantes:
- realizar pruebas al 100 % de la producción
- preservar productos estériles o de alto valor
- mejorar la trazabilidad y las investigaciones de calidad
- reducir los desechos y el coste global de la calidad
- cumplir con las normas médicas y regulatorias
Es especialmente adecuado para aplicaciones médicas de alto riesgo o reguladas.
Se utilizan varias tecnologías según la aplicación:
- Caída de presión: mide la pérdida de presión a lo largo del tiempo en dispositivos no porosos
- Caída de vacío: detecta el aumento de presión en una cámara de vacío, ampliamente utilizada para la integridad de envases estériles
- Flujo másico: mide el flujo necesario para mantener una presión objetivo
- Detección con gas trazador: ofrece una sensibilidad muy alta para aplicaciones críticas o de microfugas
Cada método se selecciona en función del material, el volumen interno, la tasa de fuga objetivo y el tiempo de ciclo.
El envasado médico estéril se prueba comúnmente mediante tecnología de caída de vacío, según lo definido en ASTM F2338.
El envase se coloca en una cámara sellada bajo vacío, y cualquier aumento de presión indica una fuga.
Este método permite:
- ensayo no destructivo
- alta sensibilidad
- cumplimiento de los requisitos de sistemas de barrera estéril
- pruebas en producción en línea o en línea cercana
Sí. El control de fugas es totalmente compatible con los marcos regulatorios médicos, incluidos:
- ISO 11607 para sistemas de barrera estéril
- ISO 13485 para sistemas de gestión de calidad
- requisitos de la FDA y del MDR, según el mercado
Los equipos de control de fugas deben validarse (IQ/OQ/PQ) y los límites de aceptación deben justificarse mediante análisis de riesgos.
Sí. Los sistemas de control de fugas pueden integrarse:
- como estaciones asistidas manualmente
- en celdas semiautomáticas
- totalmente automatizados en sistemas de producción en línea
La automatización mejora la repetibilidad, reduce la influencia del operador y garantiza una trazabilidad completa de los datos.
La sensibilidad depende de la tecnología elegida:
- los métodos de presión y vacío detectan fugas pequeñas a finas
- el caudal másico proporciona mediciones rápidas y repetibles
- los métodos con gas trazador detectan tasas de fuga extremadamente bajas
La tasa de fuga objetivo se define según el riesgo del producto, su función y su uso clínico.
No. Cuando se implementa correctamente, el control de fugas no destructivo:
- no compromete la esterilidad
- no daña el producto ni el envase
- respalda la validación de la integridad de la barrera estéril
Está diseñado específicamente para su uso en entornos controlados de fabricación médica y farmacéutica.
Los límites de aceptación se establecen durante la validación en base a:
- análisis de riesgos (ISO 14971)
- diseño y materiales del producto
- requisitos reglamentarios
- condiciones reales de uso
El límite suele correlacionarse con una fuga de referencia calibrada representativa de un modo de fallo crítico.











